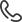Тактика консервативного ведения полного наружного послеоперационного дуоденального свища. Клинический случай
В данной статье представлен клинический случай течения и консервативного лечения полного наружного супрапапиллярного дуоденального свища, как осложнения после резекции дистальной 1/3 желудка по Бильрот 2 в модификации Бальфура, по поводу минно – взрывной травмы с проникающим ранением брюшной полости с повреждением желудка и петель тонкой кишки. Описаны использованные методы возмещения водно – электролитных и белковых потерь, нутритивной поддержки, инфузионной терапии, эфферентных методов и местного лечения. Освещаются сложности консервативного ведения данной категории больных.
Введение
Среди повреждений органов брюшной полости в результате минно – взрывных травм и огнестрельных ранений, удельный вес повреждений 12 – перстной кишки составляет от 1 до 5%. Диагностика повреждений данной локализации и выбор тактики лечения сопряжены со значительными трудностями, связанными с анатомо – физиологическими свойствами данного отдела кишечника и биомеханическими особенностями течения минно – взрывной травмы в целом. Одним из частых осложнений после экстренных операций, в числе которых встречается резекция желудка, по поводу военных повреждений желудка и 12 – перстной кишки, является наружный дуоденальный свищ, клиническое течение которого отлично, от такового при «мирных» резекциях желудка по поводу язвенной болезни, опухолей, полипов и пр. Наружные дуоденальные свищи, в том числе как осложнение оперативных пособий на желудке в объеме резекции по Бильрот – 2 в различных модификациях, и по сегодняшний день остается грозным осложнением, нередко приводящим к летальному исходу вследствие водно – электролитного истощения и полиорганной недостаточности, несмотря на множество разработанных и описанных в литературе вариантов консервативной и оперативной лечебной тактики. По данным отечественных и зарубежных исследователей частота возникновения дуоденальных свищей после резекции желудка по Бильрот – 2 колеблется от 1 до 3% [4, 5, 6]. Единого, утвержденного и однозначного алгоритма консервативного и оперативного лечения наружных свищей данной локализации не разработано и по сей день. Сложность и многополярность представленных в литературе подходов к коррекции данной патологии обусловлены гетерогенностью исследований, существенной зависимостью выбора лечебной тактики от этиологических причин формирования дуоденальных свищей и от множества сопутствующих и преморбидных исходных, в той или иной степени параллельно отягощающих течение и лечение наружных дуоденальных свищей.
Клинический случай
Военнослужащий П, 30 лет, получил проникающее осколочное ранение брюшной полости 24.12.2022г. в районе ведения боевых действий, откуда в экстренном порядке был доставлен в военный госпиталь, где был оперирован по неотложным показаниям. Была выполнена лапаротомия, ревизия органов брюшной полости, ушивание дефекта тонкой кишки (2 см от связки Трейца), резекция петли тощей кишки в связи с множественными повреждениями протяженностью 50 см (отступя 40 см от связки Трейца), ПХО входной раны передней брюшной стенки. После резекции участка тощей кишки, оральный и аборальный концы были «заглушены» линейными - механическими и кисетными швами руководствуясь принципами операций «damage control». Через 6 часов после оперативного вмешательства был доставлен в ИНВХ им. В.К. Гусака в состоянии постнаркозной депрессии, переведен в ОИТ для интенсивной терапии, динамического мониторинга. После общей стабилизации, предоперационной инфузионной и гемотрансфузионной терапии, больной был повторно оперирован через 48 часов. При ревизии, в брюшной полости патологического отделяемого не выявлено, культи тонкой кишки и место ушивания ниже связки Трейца - состоятельны. При дальнейшей ревизии выявлен сквозной дефект передней стенки пилорического отдела желудка, размерами 5 х 4 мм с неизмененными краями, ушит отдельными узловыми инвагинационными швами в два ряда. Далее, выявлен сквозной дефект области дна желчного пузыря, выполнена типичная холецистэктомия от шейки, в воротах печени – свободно лежащий металлический фрагмент неправильной полигональной формы, размерами 10 х 12 мм. Между культями тонкой кишки наложен анастомоз бок в бок отдельными узловыми инвагинационными швами в два ряда, выполнен лаваж, дренирование брюшной полости. Установлены два назогастральных зонда, проведенных за связку Трейца и в просвет желудка. Несмотря на гладкое ближайшее течение послеоперационного периода, на 4 – е сутки после второй операции отметилось обильное отделяемое по дренажам дуоденального характера, в связи с чем больной повторно оперирован в экстренном порядке. При ревизии: Место ушивания дефекта у связки Трейца, пилорического отдела желудка и энтероэнтероанастомоз состоятельны, при дополнительной широкой мобилизации желудка по большой кривизне и ревизии задней стенки выявлен дополнительный сквозной дефект пилорического отдела желудка, размерами 6 х 7 мм. Учитывая множественные повреждения с перифокальными воспалительно – инфильтративными изменениями, было принято решение повторное ушивание дефектов считать нецелесообразным, ввиду опасности несостоятельности, произведена резекция дистальной 1/3 желудка (антрумэктомия) по Бильрот – 2 в модификации Бальфура с впередиободочным Брауновским соустьем. Культя 12 – перстной кишки была ушита отдельными узловыми швами по Матешуку в два этажа. Установлены назогастральные зонды с условной маркировкой № 1 и № 2. Первый зонд проведен через гастроэнтероанастомоз, далее через отводящую петлю и Брауновское соустье к культе 12 п.к. Зонд № 2 (питательный) проведен через гастроэнтероанастомоз в отводящую петлю, ниже Брауновского соустья на 20 см. По дуоденальному зонду в первые 4 суток до 350-400 мл. На 4 – е сутки по дренажам, установленным к культе 12 – перстной кишки появилось дуоденальное отделяемое с разовым объемом 150 мл, диагностирована несостоятельность культи 12 – перстной кишки, симптомов раздражения брюшины не отмечалось, на УЗИ свободной жидкости не выявлено. Показаний к дополнительному дренированию брюшной полости не выявлено. В дальнейшем, сформировался стойкий дуоденальный свищ с ежедневным дебитом до 900 – 1500 мл/сут, жидкостных «затеков» при многократных рутинных УЗИ брюшной полости выявлено не было. При попытках подключения зонда № 1 к круглосуточной активной аспирации, дебита получено не было, вероятно из-за дренирования дуоденального содержимого через наружный свищ как кратчайший путь, так же нельзя исключить «присасывающий» эффект с перекрытием перфораций зонда стенками кишки. Пассивный ежесуточный дебит по зонду № 1 составлял ~ 50 – 100 мл. На 6 сутки, после восстановления кишечной перистальтики, начата инфузия наружных дуоденальных потерь в зонд № 2 после предварительной механической фильтрации от грубодисперсной фракции, а так же естественное дробное питание жидкой пищей, с 8 суток наладился регулярный самостоятельный стул. На 10 - е сутки для уменьшения подтекания дуоденального содержимого мимо дренажей, к последним была подключена система круглосуточной активной аспирации, дебит существенно не изменился (1200 – 1400 мл), на 24 - е сутки отключена, пассивный дебит сохранялся прежним, составлял стабильно 1000 – 1400 мл/сут. Невыраженный перифокальный ферментативный дерматит местно лечился с использованием комбинированной жирной среды «Судокрем».
С целью возмещения углеводных потерь, аминокислот и нутриционной поддержки вводилась парентеральная сбалансированная питательная смесь «Нутрифлекс 40 \ 80» из расчета рекомендованной суточной дозировки – 40 мл/кг/сут (1,6г аминокислот/кг/сут; 3,2г глюкозы /кг/сут) начиная со вторых суток от несостоятельности и на протяжении 7 суток. Подобные курсы повторялись с кратностью «неделя – через неделю». Водно - электролитный баланс компенсировался инфузией кристаллоидных и коллоидных растворов (р-р Рингера, р-р Хартмана, Трисоль, Гелофузин, Волювен и др.). Уровень протеинемии коррегировался трансфузиями иммунизированной консервированной свежезамороженной плазмы, раствором 20% альбумина человеческого, в последующем использовались спортивные протеиновые «коктейли», на фоне чего уровень общего белка находился в пределах 76 – 80 г/л. Комбинированная антибактериальная терапия в стандартных суточных дозировках препаратами группы цефалоспоринов 3, 4 поколения, аминогликозидов 3 поколения, производных имидазола, оксазолидинонов, а так же профилактическая антимикотическая терапия. На фоне переменного применения блокаторов протонной помпы и H2 – блокаторов в суточной дозе до 80 мг/сут в сочетании с атропином в дозировке 1,5 мг/сут, с целью ингибировать экзокринную функцию поджелудочной железы и гастродуоденальную секрецию, значимого эффекта не отметилось. Выполнено 6 сеансов УФО крови с целью иммуномодуляции.
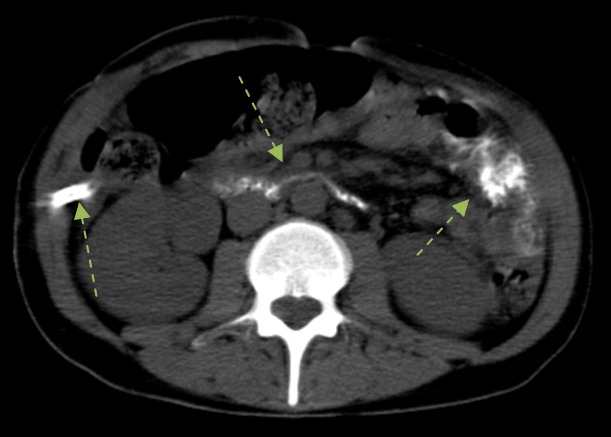
Рис. 1. СКТ + фистулодуоденография
14.02.2023г. Выполнена спиральная компьютерная томография + фистулодуоденография, ограниченных жидкостных скоплений в брюшной полости не выявлено, водорастворимый контраст, введенный в просвет дренажей, выполнил узкий свищевой ход, трубчатой конфигурации, без боковых «лакун», далее контраст выполняет просвет 12 – перстной кишки, прослеживается миграция через аорто – мезентериальный пинцет, после чего свободно выполняются петли тощей кишки (Рис. 1). Начиная с 43 – х суток после операции, выполнялась поэтапная тракция на 1 – 2 см и удаление по одному из четырех дренажей от культи 12 – перстной кишки, дебит по которым полностью прекращался. С 15.02.2023г. дебит резко снизился до 40 - 50 мл. Продолжалась поэтапная тракция оставшегося единственного дренажа, с последующим фракционным пережатием, и его удалением после полного прекращения дебита 20.02.2023г. Таким образом, на фоне описанного комплекса проведенного лечения, можно говорить о полном самостоятельном закрытии свища на 48 – е сутки, с момента несостоятельности.
Формулируя клинический диагноз, мы пользовались классификацией свищей ДПК по Саенко В.Ф. и соавт., а так же шкалой тяжести ранений 12 – перстной кишки по OIS (Organ Injury Scale), разработанной американской ассоциацией хирургов – травматологов (AAST), в 1987г.:
Послеоперационный супрапапиллярный сформированный полный трубчатый наружный конечный высокодебитный свищ 12 – перстной кишки, без дистального препятствия. Степень тяжести II по OIS.
Выводы
- Положительной стороной лечебного комплекса, представленного в данной статье, безусловно является малоинвазивность и щадящий консервативный подход, однако данные варианты закрытия свищей требуют длительного нахождения больных в стационаре.
- Описанный клинический случай наглядно демонстрирует сложности своевременной диагностики минно – взрывных повреждений желудка, 12 – перстной кишки и прилежащих органов, подчеркивает важность тщательных ревизий при первичной и повторных операциях. При одиночных или множественных ранения желудка и/или 12 – перстной кишки, следует уделять особое внимание ревизии задней стенки желудка, после предварительной широкой мобилизации его по большой кривизне, признакам повреждения задней стенки 12 – перстной кишки, к которым можно отнести «выбухание», желчное или геморрагическое пропитывание парадуоденальной париетальной брюшины, в отдельных случаях требующих мобилизации по Кохеру для прецизионной ревизии. Между тем, даже при тщательной первичной ревизии, не всегда обнаруживается сквозной дефект кишки, однако спустя 24 – 48 часов в этой же области, вследствие молекулярного сотрясения, интрамуральных микротромбозов и последующего трансмурального инфаркта стенки, он может возникнуть.
- Помимо этого, необходимо помнить, что изолированное повреждение 12 – перстной кишки встречается крайне редко, поэтому тщательному осмотру в обязательном порядке подлежат прилежащие органы (pancreas, печеночный угол ободочной кишки, желчный пузырь, правая почка, нижняя полая вена, аорта, ее парные и непарные висцеральные ветви).
- А.Н. Тулупов, В.А. Мануковский (и др.). Политравма. Руководство для врачей. 2022г. ISBN 978-5-9704-6527-1
- О.Г. Скипенко, Д.А. Чекунов, А.Л. Беджанян, Н.Н. Багмет. Наружный дуоденальный свищ. Обзор. 2016г. 10.17116/hirurgia2016886-88
- Е.Б. Городецкий, Е.Ю. Левчик. Результаты лечения несформированных боковых свищей двенадцатиперстной кишки. «Вестник хирургии». 2009г. УДК 616.342-007.253:615.036
- Orsenigo E, Bissolati M, Socci C et al. Duodenal stump fistula after gastric surgery for malignancies: a retrospective analysis of risk factors in a single centre experience. Gastric Cancer January. 2014;17(4):733- 744
- Blouhos K, Boulas KA, Konstantinidou A et al. Early rupture of an ultralow duodenal stump after extended surgery for gastric cancer with duodenal invasion managed by tube duodenostomy and cholangiostomy. Case Rep Surg. 2013
- Cozzaglio L, Coladonato M, Biffi R et al. Duodenal fistula after elective gastrectomy for malignant disease. An Italian Retrospective Multicenter Study J Gastrointest Surg. 2010;14:805-811