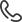ИНГИБИТОРЫ АНГИОГЕНЕЗА. СРАВНЕНИЕ РАНИБИЗУМАБА И БРОЛУЦИЗУМАБА НА ЗАГРУЗОЧНОЙ СТАДИИ ЛЕЧЕНИЯ НЕОВАСКУЛЯРНОЙ ВМД
Изучены результаты применения нового ингибитора ангиогенеза бролуцизумба в сравнении с препаратом предыдущего поколения ранибизумабом у больных с влажной формой возрастной макулярной дегенерации (ВМД).
Десяти больным с влажной формой ВМД, которые ранее не получали лечение, проводились рекомендованные три ежемесячные загрузочные интравитреальные инъекции препарата бролуцизумаб, затем интервал был увеличен до 12 недель.
После каждой инъекции проводилась оценка состояния макулярной области сетчатки по данным оптической когерентной томографии (ОКТ), ОКТ-ангиографии, прямой офтальмоскопии и биомикроскопии глазного дна с применением асферической линзы.
Проведённый анализ данных ОКТ после каждой инъекции показал более быстрое и стойкое достижение результатов (уменьшение толщины центральной зоны сетчатки, рассасывание интра- и субретинальной жидкости, жидкости под пигментным эпителием сетчатки, улучшение остроты зрения) при применении препарата бролуцизумаб в сравнении с препаратом ранибизумаб.
Изучены результаты применения нового ингибитора ангиогенеза бролуцизумба в сравнении с препаратом предыдущего поколения ранибизумабом у больных с влажной формой возрастной макулярной дегенерации (ВМД).
Десяти больным с влажной формой ВМД, которые ранее не получали лечение, проводились рекомендованные три ежемесячные загрузочные интравитреальные инъекции препарата бролуцизумаб, затем интервал был увеличен до 12 недель.
После каждой инъекции проводилась оценка состояния макулярной области сетчатки по данным оптической когерентной томографии (ОКТ), ОКТ-ангиографии, прямой офтальмоскопии и биомикроскопии глазного дна с применением асферической линзы.
Проведённый анализ данных ОКТ после каждой инъекции показал более быстрое и стойкое достижение результатов (уменьшение толщины центральной зоны сетчатки, рассасывание интра- и субретинальной жидкости, жидкости под пигментным эпителием сетчатки, улучшение остроты зрения) при применении препарата бролуцизумаб в сравнении с препаратом ранибизумаб.
Введение. Настоящим прорывом в лечении целого ряда глазных заболеваний стало появление лекарств, способных блокировать ангиогенез. В настоящее время во всём мире разработаны и применяются несколько препаратов, способные блокировать сосудистый эндотелиальный фактор роста (vascular endothelial growth factor — VEGF). VEGF — это молекула с ангиогенными свойствами, которая стимулирует митоз эндотелиальных клеток и повышает проницаемость сосудистой стенки. Разные антиангиогенные препараты блокируют разные этапы ангиогенеза: продукцию VEGF, его воздействие на рецепторы, пострецепторный сигнальный путь [1, с.12-19].
Первые опыты применения подобных препаратов в офтальмологии относятся к 2004 году. Именно тогда стали применять препарат Пегаптаниб (торговое название Макуген), который является пегилированным модифицированным олигонуклеотидом, обладающим сродством к внеклеточному изомеру VEGF 165, и способен его подавлять. Это селективный препарат с избирательным действием. Его влияние на сосудистую стенку нормальных сосудов минимально. Препарат хорошо зарекомендовал себя в терапии влажной формы ВМД. Но в дальнейшем появились новые, более эффективные препараты, и Пегаптаниб перестал использоваться [2, с.805-810].
В офтальмологии применяют следующие ингибиторы ангиогенеза: Бевацизумаб (торговое название Авастин), Ранибизумаб (торговое название Луцентис), Афлиберцепт (торговое название Эйлеа). В Российской Федерации анти-VEGF препараты применяются с 2007 года. Официальное разрешение для применения в глазной практике имеют Ранибизумаб и Афлиберцепт, в то время как Бевацизумаб в РФ не разрешён, несмотря на его популярность во всём мире [3, с. 493-497, 4, с.752-756]. Бевацизумаб (Авастин) – гуманизированное рекомбинантное моноклональное антитело. Препарат селективно связывает все изоформы VEGF и нейтрализует его. Первоначально препарат был разработан для онкологических больных и применяется до сих пор в онкологии в виде внутривенных инъекций. Первые опыты применения бевацизумаба в офтальмологии относятся к 2005 году. Чтобы уменьшить системное действие препарата, его стали вводить в стекловидное тело. Это способствовало и максимальному приближению лекарства к «мишени», каковой является неоваскулярная мембрана. Несмотря на то, что согласно инструкции, препарат не предназначен для введения в полость стекловидного тела, он является самым распространенным ингибитором ангиогенеза и широко применяется во всём мире [5, с.220-226; 6, с.1144-1167; 7, с.1296-1304].
Ранибизумаб (Луцентис) является человеческим моноклональным фрагментом антитела к эндотелиальному фактору роста А (VEGF-A). Препарат избирательно связывается с изоформами VEGF-А, предотвращая взаимодействие фактора роста с его рецепторами на поверхности клеток эндотелия сосудов. Это приводит к подавлению неоваскуляризации и пролиферации сосудов и уменьшению проницаемости сосудистой стенки. На сегодняшний день ранибизумаб - наиболее изученный ингибитор ангиогенеза. Препарат эффективен и безопасен. Он не только замедляет снижение зрения, но и частично восстанавливает его. В Российской Федерации ранибизумаб используется с 2008 года. У больных с влажной формой ВМД препарат позволяет сохранять зрительные функции в течение длительного периода времени [8, с.72-84].
Афлиберцепт (Эйлеа) – это гибридный белок, состоящий из частей внеклеточных доменов рецепторов VEGF 1 и 2. Афлиберцепт действует как растворимый рецепторный «белок-ловушка». Эффект афлиберцепта аналогичен действию ранибизумаба. Препарат эффективен в лечении влажной формы ВМД. Он уменьшает количество жидкости в сетчатке, улучшает остроту зрения и поддерживает эти эффекты в течение достаточно длительного времени. Афлиберцепт хорошо переносится пациентами. Осложнения, возникающие в процессе лечения, аналогичны нежелательным явлениям, возникающим при лечении другими анти-VEGF препаратами. Одним из преимуществ препарата является то, что для достижения стабильного эффекта требуется несколько меньшее количество его инъекций.
В 2018 году появляется препарат Бролуцизумаб (торговое название Визкью). В РФ это лекарство было допущено к использованию в 2020 году [9, с.32-39].
Бролуцизумаб — это инновационная молекула с уникальным строением, которая была специально разработана для лучшего контроля неоваскулярной ВМД. Бролуцизумаб является первым и наиболее изученным гуманизированным одноцепочечным фрагментом вариабельных доменов антитела, мишенью которого является VEGF-A. Благодаря своему малому размеру молекула бролуцизумаба способна лучше проникать через слои сетчатки, в том числе через поры в пигментном эпителии. Низкая молекулярная масса и высокая молярная концентрация Визкью способствуют достижению выраженного по скорости и длительности терапевтического эффекта. Эти свойства способствуют значимому повышению остроты зрения, лучшему рассасыванию жидкости в сетчатке, обеспечивают возможность применения препарата в режиме 1 раз в 12 недель сразу после загрузочной фазы. Препарат демонстрирует общий благоприятный профиль безопасности в течении 2 лет терапии. Режим терапии 1 раз в 12 недель позволит снизить затраты на лекарственную терапию пациентов с неоваскулярной ВМД уже в первый год использования. Использование Визкью почти на четверть сокращает число случаев госпитализации для проведения интравитреальных инъекций, что может быть использовано для проведения иных видов медицинской помощи [10, с.27-45; 11, с.24-45;].
Подводя итог, можно сказать, что в настоящее время существует группа ингибиторов ангиогенеза, применяемых для лечения влажной формы ВМД и ряда других патологических состояний центральных отделов сетчатки. Они отличаются строением молекул, физико-химическими характеристиками, но все эти препараты в исследованиях и в клинической практике показали сходные эффективность и безопасность. Все они способствуют улучшению зрения в краткосрочной перспективе, уменьшают активность неоваскулярной мембраны и снижают экссудацию. В ближайшее время благодаря развитию новых технологий будем надеется на появление новых препаратов, возможно, еще более эффективных и безопасных, чем те, что уже имеются.
Материал и методы
Для исследования были отобраны 10 ранее не получавших никакую терапию больных с неоваскулярной формой ВМД, которым мы выполнили 3 загрузочные инъекции препарата Бролуцизумаб в дозировке 0,05 мл с интервалами в 1 месяц. В другую группу были включены 10 больных с влажной формой ВМД, которым мы выполнили 3 загрузочные ежемесячные инъекции препарата Ранибизумаб в дозировке 0,05 мл. Исходные характеристики у больных из обеих групп были схожими (увеличенная толщина центральной зоны сетчатки (ТЦЗС) в среднем от 275 до 475 мкм, наличие интра- и (или) субретинальной жидкости, отслойка нероэпителия, отслойка пигментного эпителия сетчатки, наличие активной неоваскулярной мембраны).
Максимально корригированная острота зрения (МКОЗ) на момент начала терапии находилась в диапазоне 0,09-0,6 (в среднем 0,31) в группе бролуцизумаба и 00,3-0,7 (в среднем 0,34) в группе ранибизумаба. Результаты у всех больных оценивались как после каждой интравитреальной инъекции (ИВИ), так и после всей загрузочной фазы в целом. Оценивались такие параметры, как максимально корригированная острота зрения, толщина центральной зоны сетчатки, состояние интра- и субретинальной жидкости, жидкости под пигментным эпителием сетчатки. Также обращалось внимание на наличие или отсутствие нежелательных явлений (рис. 1,2,3,4).
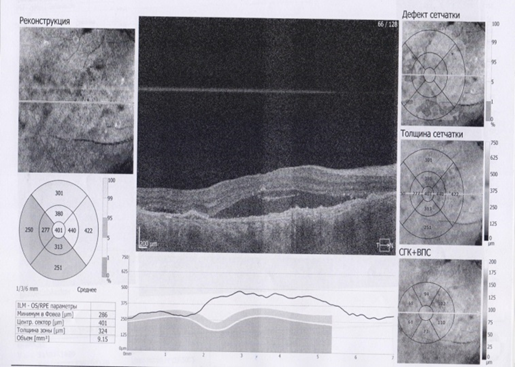
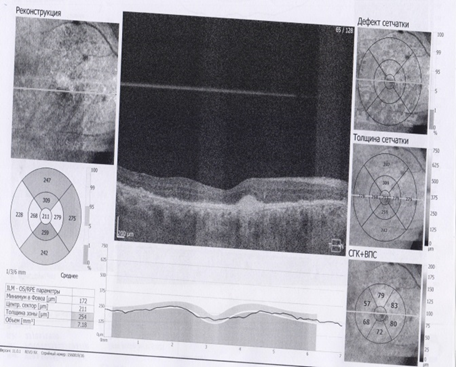
Рис.1. ОКТ макулярной области пациента А. 65 лет до (слева) и после (справа) ИВВ Визкью
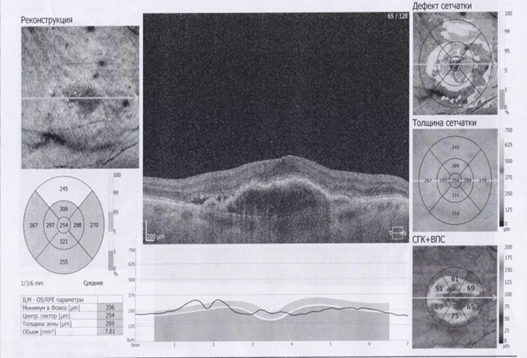
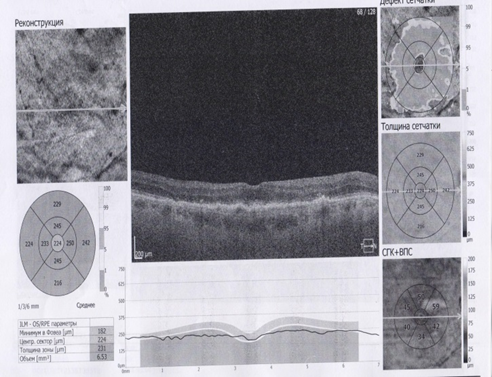
Рис.2. ОКТ макулярной области пациента Б. 71 года до (слева) и после (справа) ИВВ Визкью
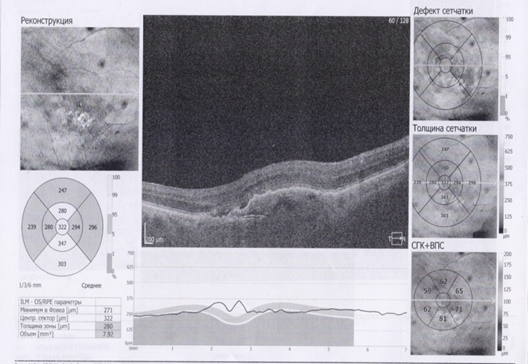
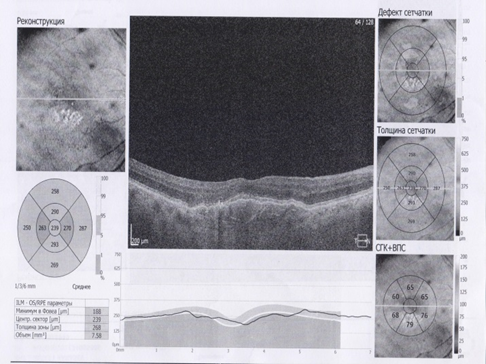
Рис.3. ОКТ макулярной области пациента В. 59 лет до (слева) и после (справа) ИВВ Визкью
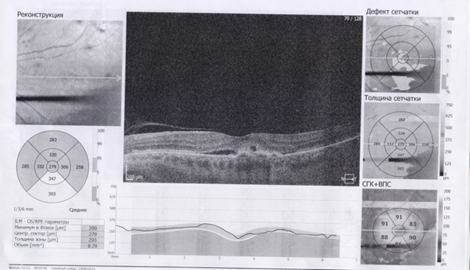
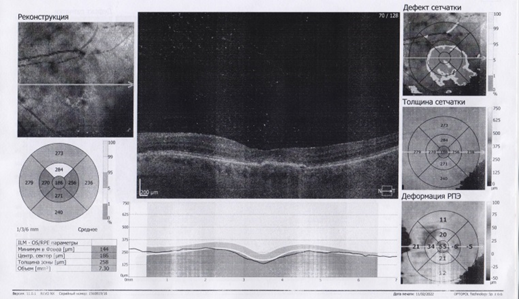
Рис.4. ОКТ макулярной области пациента Г. 76 лет до (слева) и после (справа) ИВВ Визкью
Результаты
Максимальная корригированная острота зрения.
Исходная максимально корригированная острота зрения у пациентов, получавших Бролуцизумаб, колебалась от 0,09 до 0,6 (в среднем 0,31±). После загрузочной фазы произошло улучшение остроты зрения в среднем с 0,31 до 0,6. У двух больных прирост остроты зрения происходил после 1-й инъекции, затем оставшись на новом уровне. У пяти больных происходило постепенное улучшение зрения после 2-й и 3-й инъекции. У одного больного острота зрения осталась одинаковой на протяжении всей загрузочной фазы. У двух больных зрение улучшилось после 2-й инъекции и осталось таким же после 3-й.
В группе, получавшей Ранибизумаб, исходная острота зрения колебалась от 0,03 до 0,7 (среднее 0,34). После всей загрузочной фазы МКОЗ увеличилась у 6-ти больных, осталась на прежнем уровне у трех больных, снизилась на 0,05 у одного больного (в среднем улучшилась с 0,34 до 0,35) (рис. 5).
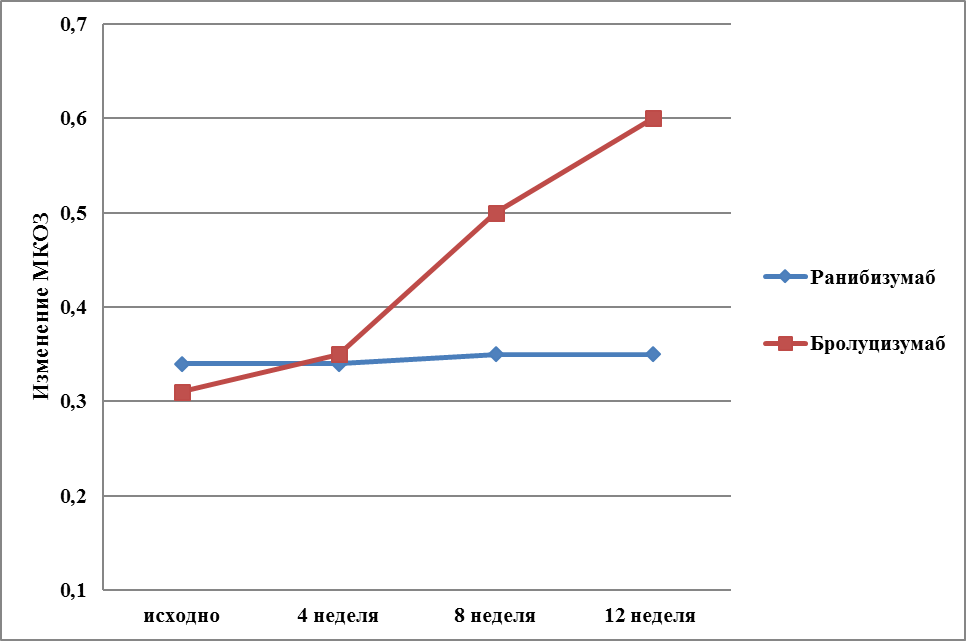
Рис. 5. Изменение максимально корригированной остроты зрения (МКОЗ)
Толщина центральной зоны сетчатки
Толщина центральной зоны сетчатки в группе Бролуцизумаба в среднем уменьшилась на 78 мкм. Уже после первой инъекции толщина центральной зоны сетчатки снизилась на 70 мкм, после второй инъекции снизилась еще на 2-3 мкм, а после третей инъекции снизалась еще на 8 мкм.
Толщина центральной зоны сетчатки в группе Ранибизумаба в среднем уменьшилась на 26 мкм (рис. 6). После первой инъекции толщина центральной зоны сетчатки снизилась на 10 мкм, после второй инъекции снизилась на 18 мкм от исходного, а после третей инъекции на 26 мкм от исходного.
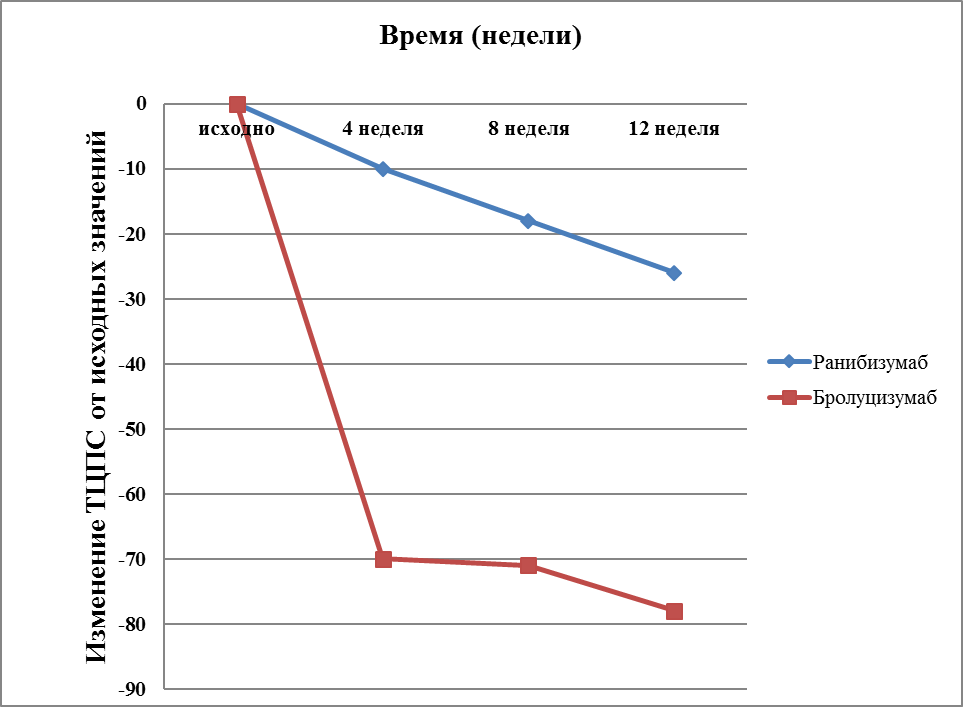
Рис. 6 Изменение толщины центральной зоны сетчатки (ТЦЗС) от исходных значений
Интраретинальная и/или субретинальная жидкость
В группе Бролуцизумаба уже после первой инъекции отмечалось значительное уменьшение интра- и субретинальной жидкости, а после всей загрузочной фазы её полное рассасывание у всех больных.
В группе Ранибизумаба происходило гораздо менее выраженное уменьшение количества интра- и субретинальной жидкости (у 80% больных). У 20% больных количество интра- и субретинальной жидкости значимо не изменилось в течение всей загрузочной фазы (рис. 7).
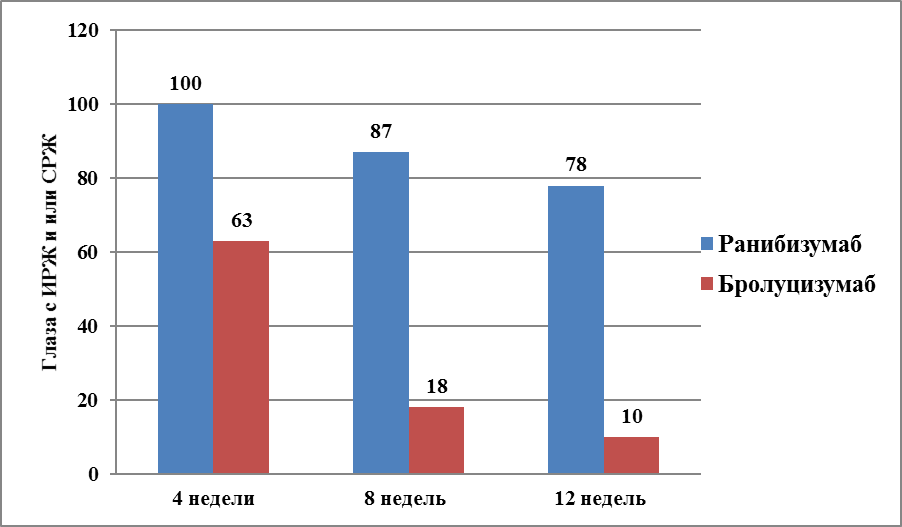
Рис. 7. Количество глаз (%) с наличием ИРЖ и/или СРЖ
Жидкость под пигментным эпителием сетчатки
Количество пациентов с жидкостью под ПЭС после загрузочной стадии в группе Бролуцизумаба составило 33%, у 67% больных жидкость рассосалась полностью.
У больных, получавших Ранибизумаб, полное рассасывание жидкости под ПЭС отмечалось у двух больных (20%). У семи больных (70%) количество жидкости под ПЭС уменьшилось. У одного больного (10%) после 3 загрузочных инъекций количество жидкости под ПЭС увеличилось, видимо за счет того, что данный препарат неэффективен в отношении этого больного. (рис. 8).
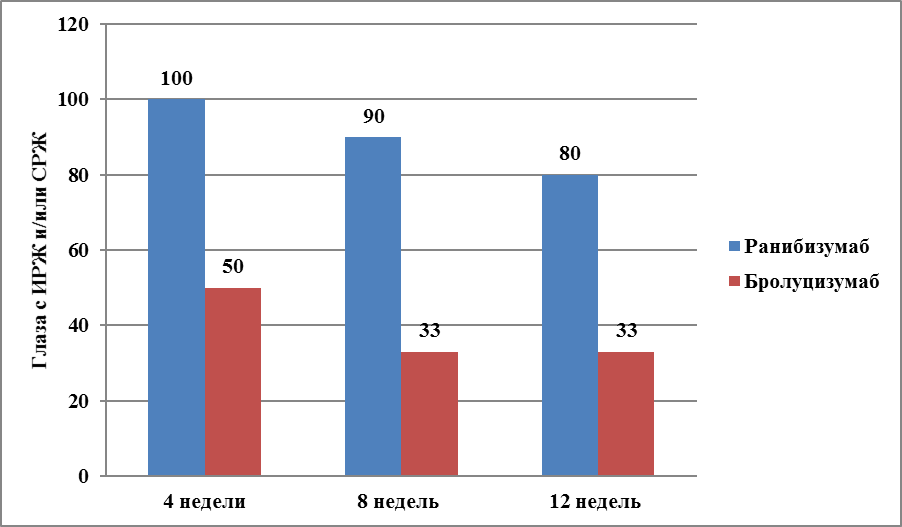
Рис.8 Количество глаз (%)с жидкостью под ПЭС
ОКТ-ангиография
Существенная динамика в группе Бролуцизумаба наблюдалась в состоянии, субретинальной неоваскулярной мембраны. Уменьшились площадь мембраны и её активность у семи больных, и полное рассасывание новообразованных сосудов у трех больных.
Данные ангио-ОКТ в группе Ранибизумаба также показали уменьшение размеров мембраны, снижение её активности у всех десяти больных.
Безопасность
В обеих группах не отмечалось никаких осложнений местного и общего характера. В двух случаях имело место субконъюнктивальное кровоизлияние и умеренное раздражение конъюнктивы, которое купировалось через несколько дней закапыванием в глаз противовоспалительных капель.
Результаты
Проведённое сравнительное исследование показывает, что в группе бролуцизумаба прирост максимальной корригированной остроты зрения превосходил аналогичный показатель в группе ранибизумаба (0,29 против 0,01 по таблице Сивцева). Причём улучшение остроты зрения в группе бролуцизумаба чаще происходило после 2-й, либо после 3-й загрузочной инъекции. После 1-й инъекции улучшение остроты зрения произошло только у двух больных из 10, и у этих двух больных она осталась на этом же уровне и после последующих инъекций. В группе ранибизумаба улучшение остроты зрения в 7 случаях произошло после 1-й инъекции, и в дальнейшем либо сохранилось (четыре больных), либо ещё улучшилось после 2-й инъекции (три больных). Снижение зрения у одного больного с 0,15 до 0,1 произошло после 3-й инъекции.
Хорошие результаты в группе бролуцизумаба наблюдались в таком анатомическом параметре, как толщина центрального подполя сетчатки. Причём изменения отмечались уже после первой инъекции, и в среднем составили 70 мкм. При этом в 7 случаях из 10 они достигли физиологических параметров после первой инъекции, и затем этот параметр либо сохранялся, либо ещё улучшился после второй и третьей инъекции. Для сравнения в группе ранибизумаба среднее уменьшение ТЦЗС составило всего 26 мкм. Уменьшение ТЦЗС в этой группе отмечалось в среднем на 5-10 мкм после каждой загрузочной инъекции (9 больных). У одного больного произошло увеличение ТЦЗС на 15 мкм после второй инъекции и осталось на этом же уровне после третьей (острота зрения у этого больного не изменилась).
У всех больных в группе бролуцизумаба отмечалось уменьшение или полное рассасывание интра- и субретинальной жидкости, а также жидкости под пигментным эпителием. Этот показатель начинал работать уже после 1-й инъекции. А после всего загрузочного цикла у 100% глаз интра- и субретинальная жидкость рассосалась полностью, а жидкость под ПЭС в небольших количествах оставалась у трети больных. В группе ранибизумаба показатели рассасывания всех видов жидкости были гораздо хуже — от полного или частичного рассасывания до сохранения примерно в тех же количествах и до увеличения в одном случае.
Так как толщина центральной зоны сетчатки и различные виды жидкости являются главными маркерами активности заболевания, следовательно, уменьшение ТЦЗС и резорбцию жидкости можно считать основными показателями эффективности лечения. Терапия бролуцизумабом обеспечивает более выраженное уменьшение проницаемости стенок сосудов и это может быть связано с уникальными характеристиками молекулы препарата: малый размер, меньшая молекулярная масса, лучшее проникновение под пигментный эпителий, длительное сохранение в очаге, более высокая терапевтическая доза.
Вместе с тем, нет полной корреляции между анатомическими параметрами и остротой зрения. У одного больного исходная острота зрения (0,1) оставалась на этом же уровне после каждой из трех инъекций, хотя толщина центральной зоны сетчатки уменьшилась на 60 мкм после первой инъекции, еще на 15 мкм после второй инъекции, и еще на 8 мкм после инъекции. Не во всех случаях резорбция жидкости и снижение толщины сетчатки в макуле сопровождались повышением остроты зрения. Но это говорит о том, что ВМД - многофакторное заболевание, а острота зрения лишь один из показателей.
В обеих группах не отмечалось серьезных осложнений за исключением субконюъктивальных кровоизлияний у двух больных. У больных, получавших и бролуцизумаб и ранибизумаб, не было замечено ни одного случая нежелательных явлений. Больные не предъявляли жалоб, данные обследований не показали симптомов воспаления переднего, среднего или заднего отрезка; не было отмечено случаев эндофтальмита, васкулита, окклюзий сосудов сетчатки и зрительного нерва, высокого ВГД. Наши наблюдения подчёркивают, что бролуцизумаб не уступает ранибизумабу в плане безопасности.
Заключение
Сравнение загрузочных фаз бролуцизумаба и ранибизумаба показывает, что бролуцизумаб позволяет добиться большего прироста остроты зрения, лучшего рассасывания интраретинальной, субретинальной жидкости и жидкости под пигментным эпителием, более значимого уменьшения толщины центральной зоны сетчатки. А сохранение всех этих показателей на первом 12-недельном интервале после загрузочного цикла позволяет надеяться, что и в дальнейшем удастся сохранить этот межинъекционный интервал, что позволит снизить затраты на лечение больных с неоваскулярной формой ВМД, и будет удобнее для самих больных.
- Оптическая когерентная томография сетчатки, под редакцией Дакера Джея С., Вэхид Надии К., Голдмана Дэрина, Москва:2019, С.12-19.
- Офтальмология: национальное руководство, под редакцией Аветисова С.Э., Егорова Е.А., Мошетовой Л.К.,. Нероева В.В, Тахчиди Х. П.. Москва: ГЭОТАР-Медиа, 2008, С. 805-810.
- Джонас Джей Б.И, генеральный директор Панда-Джонас С. Последние сведения об эпидемиологии возрастной макулярной дегенерации. Азия Пак Джей Офтальмол (Phila). 2017; 6: С. 493-497.
- Оуэн К.Г., Джаррар З., Вормальд Р. [и др.]; Предполагаемая распространенность и частота поздней стадии возрастной макулярной дегенерации в Великобритании. Br J Офтальмол. 2012; 96: С.752-756.
- Хольц Ф.Г., Тадайони Р., Битти С. [и др.]; Многолетний реальный опыт применения антисосудистого эндотелиального фактора роста для лечения влажной возрастной макулярной дегенерации. Br J Офтальмол. 2015; 99: С.220-226.
- Шмидт-Эрфурт У, Чонг В, Левенштейн А [и др.]; Руководство по лечению неоваскулярной возрастной макулярной дегенерации Европейского общества специалистов по сетчатке (EURETINA). Br J Офтальмол. 2014; 98: С.1144-1167.
- Дюгель ПУ, Яффе Дж.Дж., Саллстиг П. [и др.]; Бролуцизумаб в сравнении с афлиберцептом у участников с неоваскулярной возрастной макулярной дегенерацией: рандомизированное исследование. Офтальмология. 2017; 124: С.1296-1304.
- Дугель П.У, Ко А, Огура У [и др.]; HAWK and HARRIER: фаза 3, многоцентровая, Рандомизированные исследования бролуцизумаба с двойной маскировкой при неоваскулярной возрастной макулярной дегенерации. Офтальмология. 2020; 127 (1): С. 72-84.
- Возрастная макулярная дегенерация. Бикбов М.М., Файзрахманов Р.Р., Ярмухаметова Л.Р.. ГБУ Уфимский научно-исследовательский институт глазных болезней Академии наук Республики Башкортостан. Москва, 2013, С. 32-39.
- Возрастная макулярная дегенерация. С.А. Алпатов, А.Г. Щуко, Е.М. Урнева, В.М. Малышев. Москва, ГЭОТАР-Медиа, 2010, С.27-45.
- ОКТ сетчатки. Метод анализа и интерпретации, под редакцией В.В. Нероева, О.В. Зайцевой. Москва, 2012, С.27-45.